我国学者与海外合作者在卵巢癌免疫治疗新靶点研究方面取得进展
2025/06/02
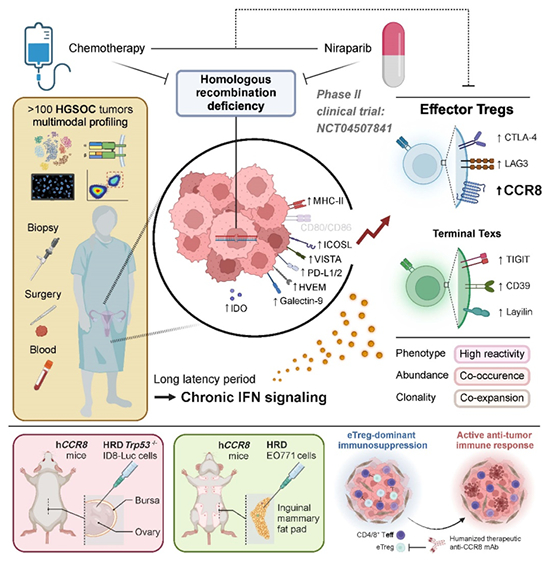 |
图 新辅助化疗或PARP抑制剂重塑HRD肿瘤免疫微环境的机制
在国家自然科学基金项目(批准号:82372928、82373332、82272707、82072889、81974405、81772787)等资助下,华中科技大学高庆蕾教授、方勇教授和马丁教授团队联合美国M.D. Anderson癌症中心梁晗教授团队在卵巢癌免疫治疗方面取得进展,研究结果以“卵巢癌新辅助PARPi或化疗揭示eTreg细胞为HRD肿瘤新靶点(Neoadjuvant PARPi or Chemotherapy in Ovarian Cancer Informs Targeting Effector Treg Cells for Homologous-Recombination-Deficient Tumors)”为题,于2024年7月5日在《细胞》(Cell)杂志上在线发表。论文链接:https://doi.org/10.1016/j.cell.2024.06.013。
卵巢癌是女性生殖系统最常见的恶性肿瘤之一,其中高级别浆液性卵巢癌(High-grade serous ovarian cancer, HGSOC)占比最高(占比70%)、恶性程度也最高。目前标准的治疗方案仍为铂类药物为主的新辅助化疗,虽然患者早期响应率较高,但容易发生耐药,五年生存率仅30%。同源重组修复缺陷(Homologous recombination deficiency, HRD)在卵巢癌中存在较为普遍,与肿瘤细胞对PARP抑制剂(PARPi)的敏感性增加有关。然而,HRD及其相关治疗对肿瘤微环境(Tumor microenvironment, TME)的影响尚不明确。
基于一项前瞻性临床试验(NANT, NCT04507841),该团队利用单细胞基因表达和T细胞受体分析发现:HGSOC中效应调节性T细胞(effector regulatory T cells, eTregs)是HRD和新辅助疗法的关键响应者,并与其他肿瘤反应性T细胞,特别是终末耗竭型CD8+ T细胞(Tex)共同存在。TME中的干扰素信号参与上调癌细胞表面MHC II类分子和其他共抑制分子,进而驱动Treg和Tex的命运。在HRD-HGSOC小鼠模型中,无论是否使用PARP抑制剂,eTregs的耗竭都能显著抑制肿瘤生长,且未观察到明显的毒性,这突出了针对eTregs的治疗策略在HGSOC和其他HRD相关肿瘤中的潜力。进一步研究发现应用CCR8单抗或CD25单抗靶向清除eTreg并联合尼拉帕利治疗HRD类型HGSOC,可取得更加显著抑瘤效果(图)。
该研究从临床问题出发,解析了PARP抑制剂和含铂类化疗药物重塑HRD-HGSOC免疫微环境的机制,并发现HRD肿瘤的免疫治疗新靶点eTreg,为HRD肿瘤免疫治疗提供了新思路。
文章来源国家自然科学基金委员会,分享只为学术交流,如涉及侵权问题请联系我们,我们将及时修改或删除。
-
2026年6月优质国际学术会议推荐 7

-
2026年第17届机械与航空航天工程 193

-
2026年先进航空航天技术与卫星应用 324

-
2026资源、化学化工与应用材料国际 1808

-
2026年图像处理与数字创意设计国际 1632

-
2026年机械工程,新能源与电气技术 6095

-
2026年材料科学、低碳技术与动力工 1819

-
2026年艺术、文化产业与数字媒体国 04-29

-
2026年智慧教育、教育研究与文化交 04-29

-
2026年数字社会、公共管理与经济学 04-29

-
2026 政务服务、数字治理与智慧城 04-28

-
2026 制冷技术、暖通设备与环境调 04-28

-
2026 轻工材料、绿色制造与循环利 04-28

-
2026 多语言智能、翻译技术与国际 04-28

-
2026 生物育种、生态种植与现代农 04-28

-
中国科协发布2025年《重要学术12

-
2026年新锐分区(原中科院期刊2595

-
2025年两院院士增选有效候选人4402

-
2025最新JCR分区及影响因子12342

-
好学术:科研网址导航|学术头条分5673

-
2025年国际期刊预警名单发布!5837

-
2025年中科院期刊分区表重磅发20812

-
吉林大学校长张希:学术会议中的提6954

-
二维超导迈斯纳效应探测研究获进展04-29

-
研究发现笼目超导体中多重范霍夫奇04-29

-
二氧化碳加氢制高碳烯烃与航煤馏分04-29

-
靶向特定蛋白互作界面抑制乙肝病毒04-29

-
研究揭示内源信使调控膜损伤与细胞04-29

-
科学家绘制大脑星形胶质细胞转录因04-29

-
上海交大Bio-X研究院石毅与合04-29

-
农科传媒 8363

-
北京易智思信息科技有限公司 8323

-
AFEW 8429

-
中南林业科技大学 2382

-
清华大学经管学院 2454

-
新加坡国际计算机科学与信息技术学 18529

-
中国医药教育协会 24225

-
中国连锁经营协会 21377

-
全球科技论坛 24373

-
qs 24294

-
北京人间远景交流有限公司 18317

-
中国江苏常州 21278

-
河海大学水利水电学院 2400

-
杭州电子科技大学自动化学院 21729

-
深圳市泰辰置业顾问有限公司 18294

-
中国人力资源开发研究会 8584

-
深圳鑫宝华防水补漏工程有限公司 21346

-
中国营养学会 21215

-
北京市计算中心 8346

-
南京大陆产业 21278























 301
301