我国学者在“肠-肺轴”调控脓毒症诱导的急性肺损伤研究方面取得进展
2025/06/02
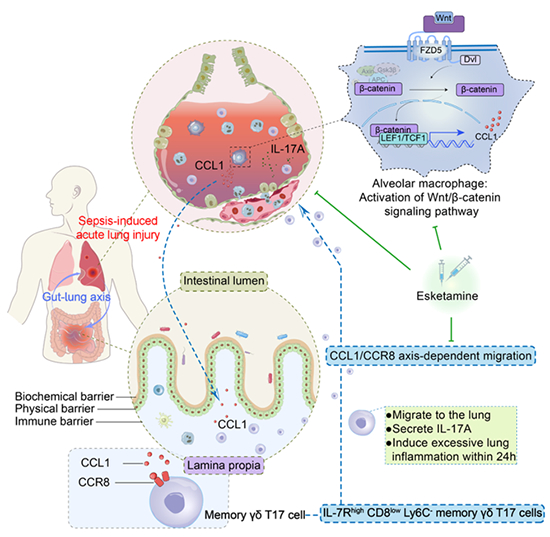
图 “肠-肺轴”调控脓毒症诱导的急性肺损伤机制及潜在的治疗策略
在国家自然科学基金项目(批准号:82071480、82272231)等资助下,华中科技大学张建成副教授、袁世荧教授与尚游教授团队在“肠-肺轴”调控脓毒症诱导的急性肺损伤研究方面取得进展。研究成果以“肠源性记忆γδ T17细胞加重脓毒症所致急性肺损伤(Gut-derived memory γδ T17 cells exacerbate sepsis-induced acute lung injury)”为题,于2024年8月7日在线发表于《自然•通讯》(Nature Communications)杂志。论文链接:https://www.nature.com/articles/s41467-024-51209-9。
脓毒症是机体对感染反应失调所致危及生命的器官功能障碍,因其引发的急性肺损伤(ALI)/急性呼吸窘迫综合征(ARDS),导致高死亡率,对人类健康造成了巨大的疾病负担。虽然“肠-肺轴”在急性肺损伤中的作用被报道,但肠道免疫细胞是否能直接迁移到肺部依然不清楚。
该研究通过对脓毒症小鼠肺组织行蛋白组学测序,发现了白介素17(IL-17)信号通路在脓毒症急性期肺部免疫失衡中起重要作用;随后采用小肠单细胞测序结合荧光小鼠光转换追踪免疫细胞技术,发现了脓毒症小鼠小肠的IL-7Rhi CD8lo Ly6Clo记忆性γδ T17细胞是肺部IL-17A的主要细胞来源,并成为脓毒症后肺部过度炎症反应和肺损伤的关键因素。进一步研究发现,脓毒症小鼠肺Wnt/β-catenin信号通路通过激活淋巴增强结合因子1(Lef1),增强肺泡巨噬细胞中趋化因子CCL1的表达,进一步介导记忆性γδ T17细胞从小肠迁移到肺部聚集并释放促炎细胞因子IL-17A,导致肺组织炎症和损伤;右旋氯胺酮(S-KT)可通过抑制肺部Wnt/β-catenin信号通路,从而抑制小肠γ δ T17细胞向肺内迁移,减轻脓毒症所致的急性肺损伤(图)。
该研究揭示了肠道来源的记忆性γδ T17细胞通过“肠-肺轴”迁移至肺部的机制,为脓毒症急性肺损伤的免疫治疗提供了新的科学依据。
文章来源国家自然科学基金委员会,分享只为学术交流,如涉及侵权问题请联系我们,我们将及时修改或删除。
-
2025第六届机械工程、智能制造与机 168

-
2025年机械工程,新能源与电气技术 171

-
2025年计算机科学、图像分析与信号 156

-
2025年材料化学与燃料电池技术国际 140

-
2025年IEEE第13届信息与通信 231

-
第十一届机械工程、材料和自动化技术国 162

-
2025培训技术、社会科学与新媒体发 06-06

-
2025教育创新、艺术与管理国际会议 06-06

-
2025生物科学、智慧医学与大数据国 06-06

-
2025神经网络、自然语言与数字孪生 06-06

-
2025智慧物联、机器视觉与交互设计 06-06

-
2025绿色材料、制造技术与机械工程 06-06

-
2025测量控制、自动识别与无人机应 06-06

-
2025工程机械、车辆工程与交通运输 06-06

-
2025电子通讯、智能电网与储能国际 06-06

-
好学术:科研网址导航|学术头条分219

-
《时代技术》投稿全攻略:一位审稿221

-
2025年国际期刊预警名单发布!349

-
2025年中科院期刊分区表重磅发3013

-
中科院已正式发布2024年预警期588

-
2025年度国家自然科学基金项目497

-
中国科协《重要学术会议目录(201657

-
2024年国家自然科学基金项目评881

-
2024年JCR影响因子正式发布853

-
吉林大学校长张希:学术会议中的提1078

-
【院校速递】今日院校科研十大要闻06-06

-
《ANNALES MEDICO-06-06

-
《ANNALES POLONIC06-06

-
《ANNALES SCIENTI06-06

-
《ANNALES D ENDOC06-06

-
国际工学技术出版协会 23844

-
北京市北京大学 17916

-
北京两岸行经济文化交流有限公司 17846

-
中国医药教育协会 1837

-
省会议接待服务中心 22882

-
CC 7924

-
大连交通大学 20886

-
中国岩石力学与工程学会 20894

-
全国微创整形外科工作委员会 24014

-
中国化工企业管理协会 23875

-
山东大学计算机科学与技术学院 22885

-
美国科研出版社 1935

-
清华设计院文化遗产保护中心洞天福 24032

-
沈阳博思教育咨询有限公司 18025

-
优势会展公司 17851

-
中国环境科学学会 20909

-
中国生态学学会专业委 17900

-
武汉大学软件工程国家 17952

-
辽宁省医学会学术部 17918

-
深圳汉威展览策划有限公司 17883



















 28
28