肠道病毒脱壳机制研究取得进展
2026/01/08
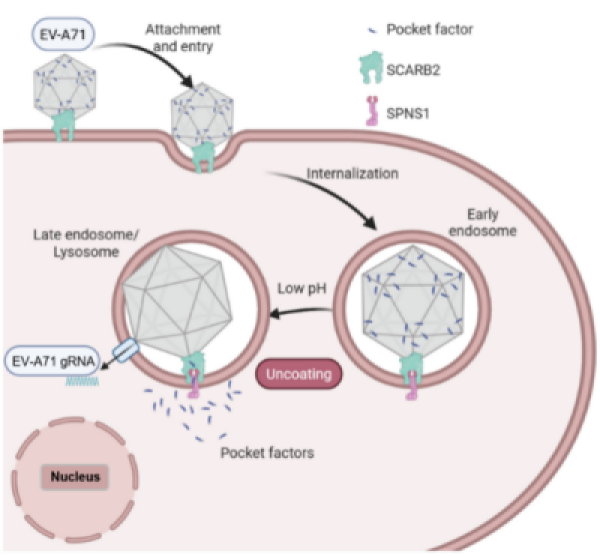
肠道病毒71型(EV-A71)病毒成功入侵细胞的核心步骤之一,在于将其基因组RNA释放至细胞质,此过程称为脱壳。研究表明,EV-A71病毒颗粒内部存在被称为“口袋因子”的鞘脂类分子,该分子对于维持病毒结构的稳定具有重要作用。在感染后,“口袋因子”需在溶酶体中被移除,以触发病毒结构蛋白解离并释放RNA。然而,“口袋因子”自溶酶体中被移除后的具体转运机制仍不明确。
近日,中国科学院武汉病毒研究所研究团队揭示,宿主细胞内的溶酶体膜蛋白SPNS1可作为病毒“口袋因子”的转运体,介导其释放,从而启动病毒脱壳过程。该发现为阐明肠道病毒感染的关键机制提供了新视角,也为防治手足口病等疾病提示了潜在的新型药物靶点。
研究团队利用CRISPR-Cas9策略,筛选了支持EV-A71感染的宿主关键因子,鉴定了溶酶体膜蛋白SPNS1为EV-A71的重要宿主因子。SPNS1是一种已知的溶酶体脂质转运蛋白,负责将如溶血磷脂等脂类分子从溶酶体腔转运至细胞质。研究人员发现,在SPNS1基因敲除的细胞中,EV-A71的感染被明显抑制。为进一步阐明其作用分子机制,研究人员用叠氮标记了EV-A71病毒的“口袋因子”,并基于点击化学—铜离子催化的叠氮—炔烃环加成反应追踪“口袋因子”的位置。
在正常细胞中,病毒感染后,“口袋因子”从溶酶体内转移并扩散至细胞质,标志着“口袋因子”的成功释放与转运。而在SPNS1缺陷的细胞中,“口袋因子”始终局限于溶酶体中,病毒脱壳过程受阻,这直接证实了SPNS1是“口袋因子”溶酶体转运的关键执行者,且SPNS1的转运活性依赖于溶酶体的酸性环境。进一步研究表明,SPNS1通过其跨膜螺旋形成的特异性结构域识别并结合“口袋因子”。SPNS1的特定关键氨基酸残基(如R76和H427)对其转运功能至关重要,这些位点的突变会使SPNS1丧失支持病毒感染的能力。
相关研究成果发表在《美国国家科学院院刊》(PNAS)上。研究工作得到国家自然科学基金委员会等的支持。
SPNS1介导EV-A71“口袋因子”释放模式图
文章来源武汉病毒研究所,分享只为学术交流,如涉及侵权问题请联系我们,我们将及时修改或删除。
-
2026年6月优质国际学术会议推荐 7

-
2026年第17届机械与航空航天工程 193

-
2026年先进航空航天技术与卫星应用 324

-
2026资源、化学化工与应用材料国际 1808

-
2026年图像处理与数字创意设计国际 1632

-
2026年机械工程,新能源与电气技术 6095

-
2026年材料科学、低碳技术与动力工 1819

-
2026年艺术、文化产业与数字媒体国 04-29

-
2026年智慧教育、教育研究与文化交 04-29

-
2026年数字社会、公共管理与经济学 04-29

-
2026 政务服务、数字治理与智慧城 04-28

-
2026 制冷技术、暖通设备与环境调 04-28

-
2026 轻工材料、绿色制造与循环利 04-28

-
2026 多语言智能、翻译技术与国际 04-28

-
2026 生物育种、生态种植与现代农 04-28

-
中国科协发布2025年《重要学术12

-
2026年新锐分区(原中科院期刊2595

-
2025年两院院士增选有效候选人4402

-
2025最新JCR分区及影响因子12342

-
好学术:科研网址导航|学术头条分5673

-
2025年国际期刊预警名单发布!5837

-
2025年中科院期刊分区表重磅发20812

-
吉林大学校长张希:学术会议中的提6954

-
二维超导迈斯纳效应探测研究获进展04-29

-
研究发现笼目超导体中多重范霍夫奇04-29

-
二氧化碳加氢制高碳烯烃与航煤馏分04-29

-
靶向特定蛋白互作界面抑制乙肝病毒04-29

-
研究揭示内源信使调控膜损伤与细胞04-29

-
科学家绘制大脑星形胶质细胞转录因04-29

-
上海交大Bio-X研究院石毅与合04-29

-
中纤网 24629

-
湖北杰瑞文化传播有限公司 23447

-
北京中工大厦 2269

-
ghr 24437

-
农业部中国农村杂志社 23242

-
WW 8154

-
上海首美展览有限公司 8162

-
中国兵工学会测试技术专业委员会 23372

-
百奥泰国际会议(大连)有限公司 24335

-
北京申雅国际会展有限公司 24346

-
云南大学 18426

-
聚氨酯研发中心 18155

-
深圳翰宇药业 21328

-
中国环境科学学会 24406

-
博锐国际展览有限公司市场部 8302

-
新疆燕泰会议服务有限公司 18360

-
昆明兴达会议服务公司 23248

-
揚州市可瑞爾公司 18302

-
北京贝拓会展 18380

-
南京医格尔信息科技有限公司 2173






















 112
112