清华大学药学院张从刚课题组揭示免疫“第二信使”cGAMP双向跨膜转运的新机制
2024/04/26
近日,清华大学药学院张从刚研究员课题组发现人类宿主防御肽LL-37是一种高效的cGAMP转运体,可以通过与cGAMP特异性结合从而双向跨细胞膜转运cGAMP,传播和放大“第二信使”cGAMP携带的免疫信号,进而在靶细胞内激活强烈的STING信号以及干扰素介导的宿主抗病毒免疫。这是迄今为止首次发现人体内溶解性多肽可以跨膜转运免疫递质cGAMP,这一发现揭示了机体抵御病毒感染的独特机制,同时为困扰人类几十年的问题“维生素D究竟如何抗病毒”提供了分子机制方面的新解释,也为疫苗研发和免疫治疗提供了新靶点和新思路。
在哺乳动物天然免疫系统中,来源于肿瘤或微生物的胞质DNA可激活cGAS合成第二信使—2’, 3’-cGAMP1,2(cGAMP)。cGAMP与STING结合使其形成二聚体,招募TBK1,磷酸化并激活IRF3,诱导I型干扰素和其他细胞因子的表达。cGAMP-STING免疫信号通路在机体抗肿瘤和抗感染等过程中发挥着非常重要的作用。
肿瘤细胞和感染细胞中的的cGAMP往往需要转移到“旁观者”细胞中,从而全局性地调动STING介导的干扰素反应和抗肿瘤/抗病毒免疫。此外,免疫治疗中使用的外源cGAMP以及其它一些由细菌产生的环二核苷酸(如3’, 3’-cGAMP)也需穿过细胞膜来激活机体多细胞免疫反应。然而,由于cGAMP带负电且具有高度亲水性,导致其很难自发穿过磷脂双层进入靶细胞内发挥作用。因此,研究cGAMP的跨膜运输对阐明宿主免疫防御机制和改善cGAMP免疫治疗效果都具有极其重要的意义。近年来,科学家逐步发现细胞间gap junction3和细胞膜上阴离子通道蛋白(SLC19A14和LRRC85)可以作为cGAMP的跨膜转运系统。但是,机体内是否存在溶解性的、游离的蛋白或多肽参与cGAMP跨膜转运目前尚不清楚。
该研究团队通过大范围筛选成功鉴定到一条人类细胞中的游离多肽LL-37可协助cGAMP进入细胞。LL-37是Cathelicidin抗菌肽家族的唯一人类成员,具有抗菌、抗病毒、免疫调节、促进伤口愈合等多种生物学功能。研究者发现,在LL-37的协助下,cGAMP能够强烈激活STING信号通路,并诱导大量的IFNβ的产生(图1)。
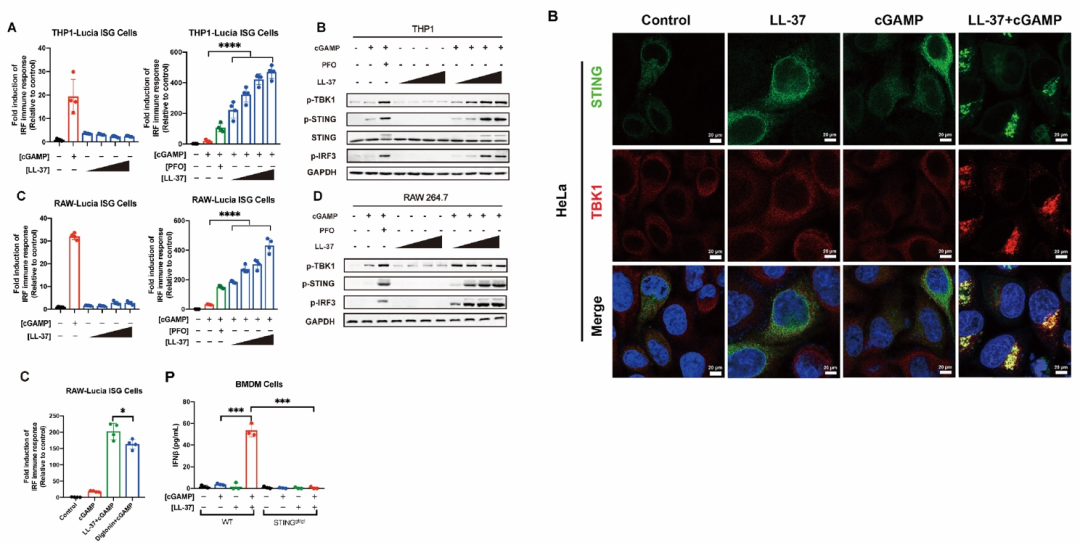
图1. LL-37促进cGAMP强烈激活STING信号通路和干扰素反应
为了进一步探究机体内源性LL-37是否也可以发挥相似的功能,研究者用两种LL-37诱导剂(维生素D [VD3] 和丁酸钠 [SB])诱导内源LL-37的表达。结果表明,VD3和SB都能够显著增强cGAMP介导的STING信号通路的激活。然而,当敲除LL-37基因后,VD3和SB对cGAMP免疫反应的增强作用完全丧失,表明VD3和SB通过诱导内源LL-37表达促进cGAMP介导的STING信号传导(图2)。前人研究表明,人体上皮细胞、唾液以及感染或炎症部位的LL-37浓度可达2-12μg/ml。该研究团队证明,此生理浓度下的LL-37足以有效促进cGAMP诱导的免疫反应,同时强效抑杀G+和G-致病菌。
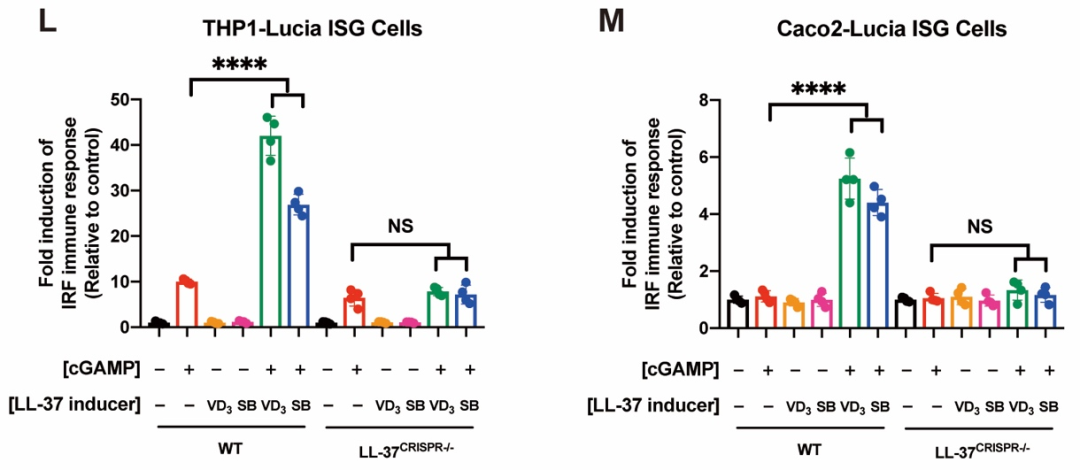
图2. VD3和SB通过诱导内源LL-37表达促进cGAMP介导的STING信号激活
接着,该研究团队通过精妙的细胞间cGAMP转移试验以及ITC、MST等试验发现LL-37通过与cGAMP特异性结合从而对cGAMP进行跨细胞膜运输(图3)。
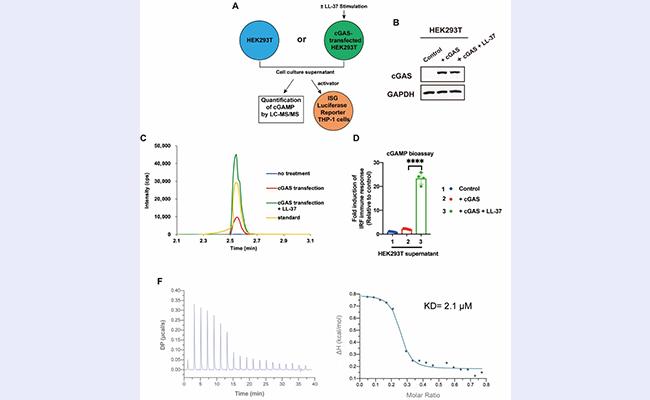
图3. LL-37通过与cGAMP特异性结合双向跨膜转运cGAMP
此外,该研究团队发现LL-37显著增强了cGAMP介导的宿主抗病毒免疫。研究者发现LL-37强烈促进了cGAMP诱导的ISG相关基因的表达(图4F)。此外,LL-37-cGAMP明显增加了小鼠血清中的IFNβ和CXCL10水平(图4G)。与单独使用cGAMP或LL-37相比,cGAMP-LL-37能够更好地缓解HSV-1诱导的小鼠体重下降症状(图4C)。更重要的是,LL-37-cGAMP组合几乎完全消除了THP1细胞(图4A和4B)和小鼠脾脏(图4D和4E)中的病毒感染。
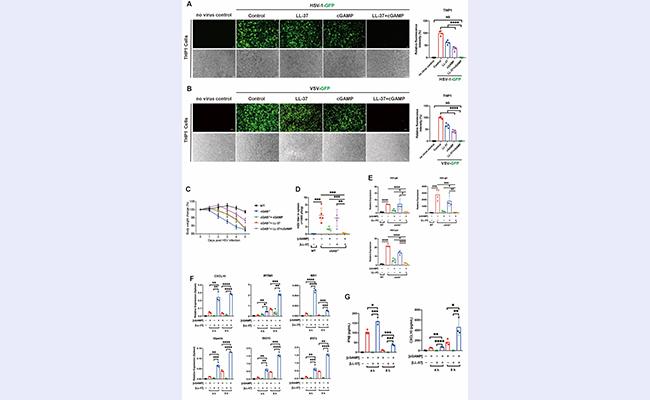
图4.LL-37-cGAMP可以强烈激活宿主抗病毒免疫
研究表明补充VD3可以增强基于IFNβ的抗病毒反应,并有证据显示补充VD3甚至可以缓解SARS-CoV-2诱发的急性呼吸道综合征。尽管早有研究报道VD3能够诱导内源性LL-37的产生,但尚不清楚VD3诱导的LL-37表达与IFNβ介导的抗病毒反应之间是否存在联系。该研究证明,VD3通过诱导内源LL-37的表达,促进了cGAMP的跨膜转运,从而高效激活STING信号通路并促进IFNβ介导的抗病毒免疫反应,解开了这个困扰人类几十年的谜题。
综之,该研究首次发现人类宿主防御肽LL-37可作为cGAMP的转运体高效激活STING介导的先天免疫反应(图5),为机体免疫调节和抗感染机制提供新的见解,并为临床免疫治疗提供了新思路。
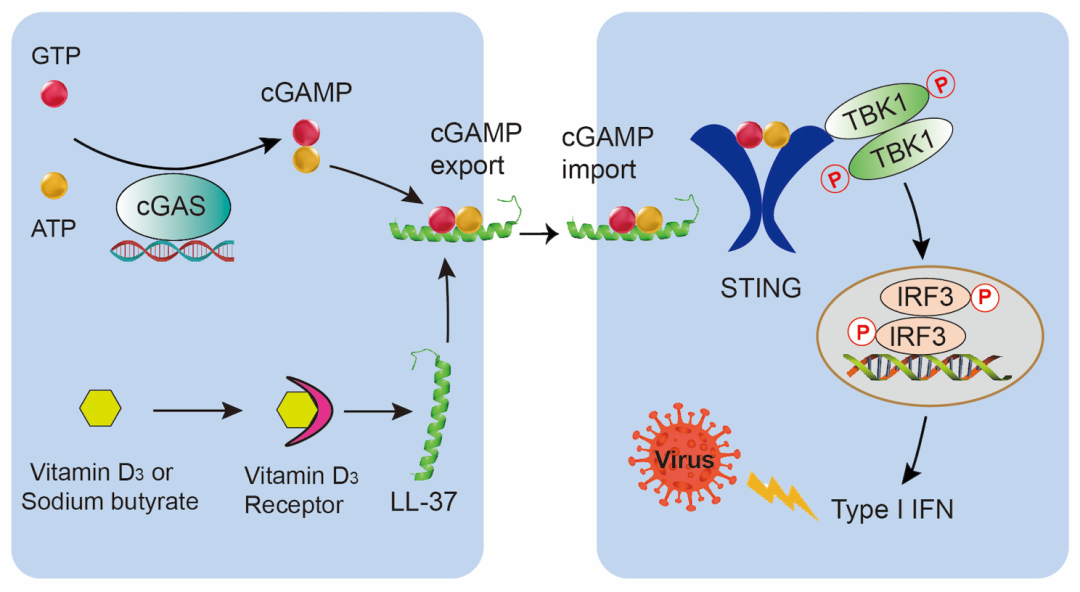
图5. LL-37跨膜转运cGAMP以激活STING信号通路并增强IFN介导的宿主抗病毒免疫的示意图
上述研究于5月31日在《细胞报道》(Cell Reports)期刊发表,标题为“LL-37转运cGAMP激活STING信号,增强干扰素介导的宿主抗病毒免疫”(LL-37 transports immunoreactive cGAMP to activate STING signaling and enhance interferon-mediated host antiviral immunity)。
清华大学药学院张从刚研究员和上海交通大学基础医学院孙序序研究员为该论文通讯作者,张从刚课题组博士后卫旭彪和张璐璐为该论文第一作者。该研究得到了国家自然科学基金项目、清华-北大生命科学联合中心、中国博士后科学基金以及上海东方学者基金的资助。
文章来源清华大学新闻,分享只为学术交流,如涉及侵权问题请联系我们,我们将及时修改或删除。
-
2025年智能光子学与应用技术国际学 06-10

-
2025年8月优质学术会议推荐 589

-
2025年第十二届能源与环境研究国际 400

-
2025年机械工程,新能源与电气技术 559

-
2025年计算机科学、图像分析与信号 553

-
2025年材料化学与燃料电池技术国际 493

-
第七届精神病学国际大会(CP 202 08-01

-
第七届老龄化与老年医学国际学术会议( 08-01

-
第十四届心理学与健康国际学术研讨会( 08-01

-
第七届测绘与地理信息国际研讨会(CS 08-01

-
第七届大气与海洋科学国际研讨会(SA 08-01

-
第十一届地质灾害研究与防治国际学术会 08-01

-
第十六届地质和地球物理学国际会议(I 08-01

-
第七届细胞科学与再生医学国际研讨会( 08-01

-
第七届合成生物学与生物医学国际研讨会 08-01

-
2025最新JCR分区及影响因子1939

-
好学术:科研网址导航|学术头条分468

-
《时代技术》投稿全攻略:一位审稿499

-
2025年国际期刊预警名单发布!600

-
2025年中科院期刊分区表重磅发3957

-
中科院已正式发布2024年预警期861

-
2025年度国家自然科学基金项目727

-
中国科协《重要学术会议目录(202733

-
2024年国家自然科学基金项目评1138

-
2024年JCR影响因子正式发布1214

-
吉林大学校长张希:学术会议中的提1391

-
SCI论文插图全攻略:从规范解析08-01

-
国际学术会议参加经验是怎么样的呢08-01

-
掠夺性会议是怎么进行判断的呢?—08-01

-
SCI论文投稿费怎么交?202408-01

-
中华两岸经贸繁荣促进会北京办事处 22950

-
APISE 23029

-
天津市塘沽区土地中心 17873

-
中国日用化学工业信息中心 18105

-
中国环境科学学会 23180

-
中国传媒大学 21067

-
HKSME 23049

-
数理科学新理论推广中心实践基地 8008

-
亚太科学与工程研究所 2021

-
星河系教育 1979

-
San Jose State U 2077

-
中建政研信息咨询中心 21093

-
生物谷 20809

-
中国化工学会 21088

-
赛特数码有限公司 17917

-
上海蔚有文化传媒有限公司 8467

-
北京大学信息学院 17962

-
北京大学计算机系 18152

-
清华大学出版社 20958

-
中国科学院电子学研究所 23406



















 653
653













































