上海交大药学院马步勇课题组:破解阿尔茨海默病关键毒性结构和抗体识别机制
2026/04/20
阿尔茨海默病(AD)是最常见的神经退行性疾病之一,其典型分子标志为β淀粉样蛋白(Aβ)的异常聚集。近年来,大量研究表明,相较于沉积形成的淀粉样纤维,Aβ寡聚体被认为是主要的神经毒性来源。Aβ寡聚体毒性的一种特殊机制是细胞膜穿孔,这种穿孔会破坏离子稳态,进而导致突触功能障碍和细胞死亡。作为细胞膜的重要组成成分,胆固醇已被证实可促进Aβ₁₋₄₂的成核聚集,从而加剧神经毒性。与此一致,中年期高胆固醇血症也被公认为阿尔茨海默病的一个重要风险因素,其与AD患病概率密切相关。
清除Aβ聚集体,尤其是寡聚体,已成为AD的一项重要的治疗目标。尽管水相中Aβ₁₋₄₂的纤维状结构已得到阐明,但其寡聚体结构仍鲜为人知。由于缺乏高分辨率结构信息,人们对于其毒性来源及作用机制仍缺乏清晰认知,药物研发也困难重重,目前仅有三款获批抗β淀粉样蛋白抗体,其临床疗效差异显著,率先获批的阿杜卡单抗很快退市。抗体识别不同Aβ寡聚体的分子机制尚不明晰,且缺乏抗体-寡聚体复合物实验结构,严重制约AD理性药物设计。
近期,上海交通大学药学院马步勇团队在《Aggregate》上发表了题为“Structure and Dynamics of Lipid-Stabilized Amyloid Beta Aβ₁₋₄₂ Oligomers”的研究论文。该研究通过整合傅里叶变换红外光谱(FTIR)、固态核磁共振(ssNMR)(图1)、透射电子显微镜(TEM)(图2)和分子动力学模拟(MD)等多维度技术,首次揭示了脂质稳定化的Aβ₁₋₄₂八聚体结构、动态特征及其神经毒性机制。研究团队解出了一种全新的Aβ寡聚体构象结构,研究发现,Aβ₁₋₄₂在含胆固醇的脂质双层中形成独特的”寿司卷”折叠结构(图3),其核心特征为:(1)通过脂质填充的疏水腔稳定八聚体构象;(2)N端与C端通过三个关键残基接触形成盐桥网络;(3)脂质-肽相互作用导致脂质体膜穿孔。该结构显著区别于传统提出的β-桶(β-barrel)水孔模型,后者通常假设孔道内部为水相环境。实验与分子动力学模拟结果显示(图3),该类寡聚体能够深度嵌入脂质双层,并与脂肪酸链发生直接相互作用。研究提出一种新的作用机制:Aβ寡聚体通过与脂质分子的协同组装,将部分脂质“捕获”并整合进自身结构,从而削弱膜的稳定性,最终导致细胞膜破坏。
该项研究首次解析了一种新型脂质稳定的Aβ₁₋₄₂分子结构,为深入理解Aβ通过神经元膜穿孔引发神经毒性提供了重要线索。研究突破了传统Aβ寡聚体结构认知,并揭示了胆固醇通过促进Aβ八聚体形成加剧疾病进展的分子机制,为理解阿尔茨海默病神经毒性提供了新视角。该成果对开发靶向Aβ-脂质相互作用的新型治疗策略具有重要指导意义。
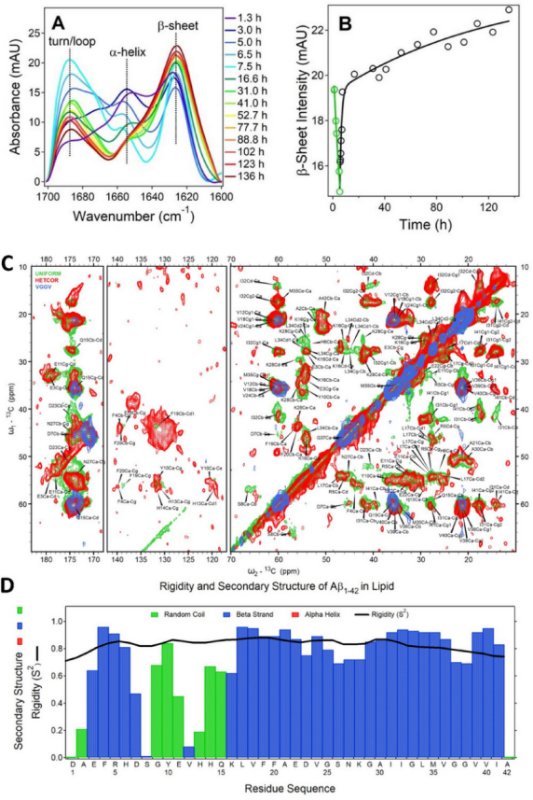
图1. FTIR光谱学和核磁共振实验研究Aβ₁₋₄₂组装囊泡的在脂膜中的结构演变。
FTIR显示β-折叠结构在5小时后呈现双指数增长,表明Aβ₁₋₄₂经历动态构象转变。NMR谱图通过VGGV标记肽段验证了38个残基的化学位移分配,揭示N端短β-链与C端长β-链的二级结构特征。
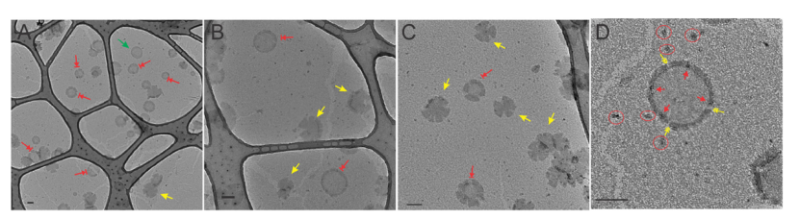
图2透射电镜观察Aβ₁₋₄₂诱导脂质囊泡损伤。
对比纯LUVs(完整球形结构)与Aβ-42重组LUVs,后者出现三种形态:完整但膜表面有孔洞的囊泡(红色箭头)、完全破裂呈花瓣状的囊泡(黄色箭头),以及嵌入囊泡壁的Aβ聚集体(红色圆圈),证实Aβ₁₋₄₂通过脂质提取机制破坏膜完整性。
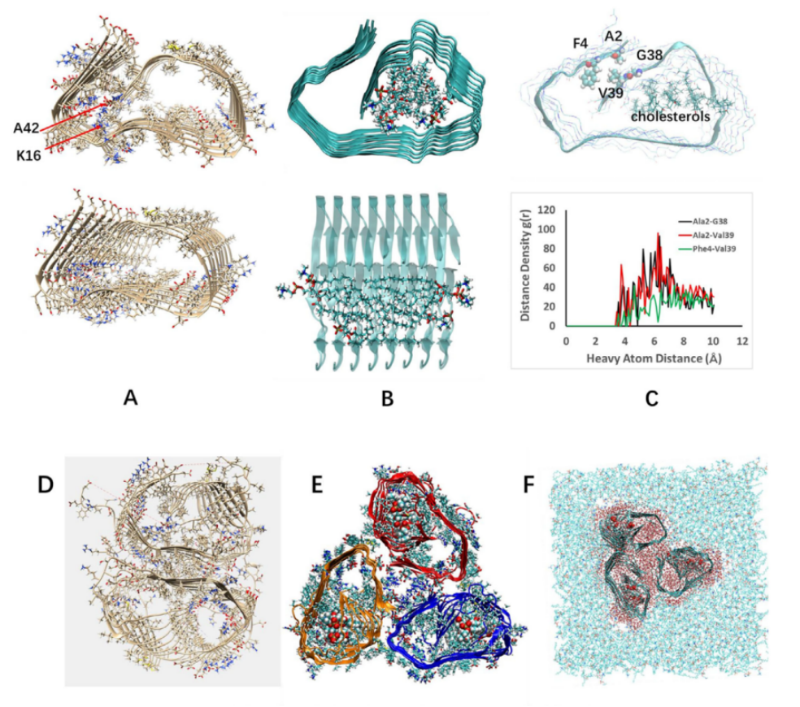
图3. 全新的脂质稳定的Aβ₁₋₄₂寡聚体“寿司卷”结构模型。
顶部视图显示交叉β-折叠结构(A),侧面视图揭示POPC脂质分子填充的疏水孔道(B)。胆固醇稳定模型显示Ala2-Gly38、Ala2-Val39、Phe4-Val39三组残基间短程接触(<4Å),支撑N端与C端相互作用的结构特征(C)。两个八聚体二聚体通过两倍旋转对称关系连接形成的八聚体二聚体(D); 三个八聚体在水中形成的三聚体,水分子渗透至脂质双层(红色点),揭示脂质-肽相互作用的动态特性(E);Aβ寡聚体嵌入脂质双层并与脂质分子相互作用示意图(分子动力学模结果)(F)上海交通大学博士后鲁慧霞和美国中佛罗里达大学Tyrone Thames博士为论文的共同第一作者;通讯作者为上海交通大学马步勇教授以及美国中佛罗里达大学的Suren Tatulian教授和陈博教授。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/agt2.70266
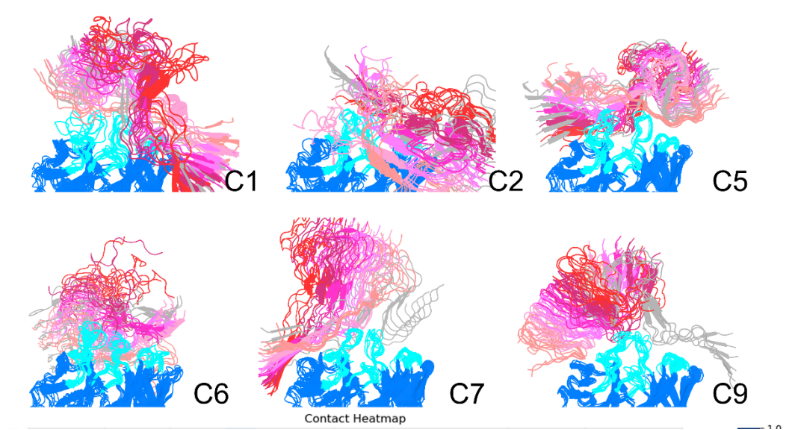
在抗体识别寡聚体的机制方面,马步勇团队随后在《International Journal of Biological Macromolecules》上发表了题为“Differential conformational selections of three therapeutic antibodies binding to polymorphic Aβ oligomers”的研究论文。通过微秒级分子动力学模拟,系统解析阿杜卡单抗、仑卡奈单抗、多奈单抗与三种Aβ寡聚体的差异化结合机制。阿杜卡单抗呈现多态体依赖性结合,靶向全长Aβ的N端表位,同时可与高度稳定的cross-β结构形成非特异性结合;仑卡奈单抗同时结合多条Aβ链的N端区域,呈现出独特的扁平结合模式(图4);多奈单抗以保守的CDRL1区域识别Aβ的F4–H13区域,且焦谷氨酸化修饰的第3位残基(pE3)可作为结构锚点,增强抗体与寡聚体的结合稳定性。上述结构层面的发现,为三款抗体的临床疗效差异提供了分子层面的解释,为开发更高效、精准的AD免疫治疗药物奠定关键基础,助力阿尔茨海默病精准治疗迈入新阶段。
图4.仑卡奈单抗与 Aβ1-42 六聚体的多模态结合模式
上海交通大学博士生徐泓淋为第一作者;通讯作者为上海交通大学马步勇教授。
文章来源上海交大,分享只为学术交流,如涉及侵权问题请联系我们,我们将及时修改或删除。
-
2026年4月高录用检索快国际学术会 564

-
2026年第17届机械与航空航天工程 152

-
2026年先进航空航天技术与卫星应用 293

-
2026资源、化学化工与应用材料国际 1776

-
2026年图像处理与数字创意设计国际 1603

-
2026年机械工程,新能源与电气技术 6073

-
2026年材料科学、低碳技术与动力工 1797

-
2026 先进材料、增材制造与装备升 04-24

-
2026 云计算、大数据平台与信息系 04-24

-
2026 地质工程、矿产资源与绿色开 04-24

-
2026 虚拟现实、增强现实与数字孪 04-24

-
2026 园林工程、生态绿化与城市景 04-24

-
2026 影视传媒、动画设计与数字文 04-24

-
2026 数学建模、仿真分析与工程计 04-24

-
2026 数控技术、机械加工与智能装 04-24

-
2026年中科院期刊分区表(新锐2455

-
2025年两院院士增选有效候选人4381

-
2025最新JCR分区及影响因子12246

-
好学术:科研网址导航|学术头条分5631

-
2025年国际期刊预警名单发布!5792

-
2025年中科院期刊分区表重磅发20538

-
中国科协《重要学术会议目录(2011707

-
吉林大学校长张希:学术会议中的提6912

-
科学家利用重离子辐照技术创制新型04-25

-
“双面胶”疗法为高效对抗白血病提04-25

-
科学家提供阿尔茨海默病治疗新策略04-25

-
西北农林科技大学全国政协委员昝林04-25

-
西北农林科技大学(807)动科学04-25

-
西北农林科技大学(808)园艺学04-25

-
西北农林科技大学(809)资环学04-25

-
沈阳航空工业学院 23413

-
南京财经大学 23410

-
上海广贸会展服务有限公司 23513

-
中国发展战略学研究会企业战略专业 18385

-
《工程力学》杂志社 18309

-
化工有限公司 18224

-
中国海洋石油总公司 24352

-
清华大学 8322

-
吉林大学 21368

-
北京艾尚国际展览有限公司 8189

-
沈阳博思有限公司 18270

-
一码通天下信息技术投资有限公司 21188

-
重庆文理学院 18283

-
国际科学与工程发展协会 23450

-
同济大学 21483

-
四川大学 21434

-
飞鸟科技 21666

-
西安连成行管理有限物业 21259

-
国际工学技术出版协会 8201

-
北京沃玉科技发展中心 8530























 20
20