清华大学 药学院鲁白团队开发新的人源性阿尔茨海默病类脑器官模型并确定APOE3ch突变对该病的保护性作用
2024/05/14
阿尔茨海默病(AD)是一种神经退行性疾病,表现为认知功能减退以及行为与性格改变。AD具有遗传倾向,致病基因的罕见突变会直接导致常染色体显性遗传AD的发生,如APP(β-淀粉样蛋白前体)基因、PSEN1(早老素1)基因和PSEN2(早老素2)基因等。在病理层面,细胞外的β-淀粉样蛋白(Aβ)斑块沉积与细胞内的tau蛋白纤维缠结是AD的两大主要病理特征。通过遗传学研究,可以解析导致AD的关键基因以及这些基因在AD发展中的作用,对于理解AD的发病机制和开发治疗策略具有重要意义。
载脂蛋白E(APOE)基因多态性是散发性AD发生的主要遗传风险因素,与常见的APOE变体(variant)APOE*ε3相比,APOE*ε4等位基因会导致罹患AD的风险大大增加,而APOE*ε2等位基因会降低AD风险。在世界上最大的阿尔茨海默病常染色体显性遗传家系中,有一位PSEN1 E280A携带者的认知减退发生年龄推迟近30年,且脑中tau蛋白病理显著降低。全外显子测序数据揭示APOE3的罕见纯合突变APOE3 Christchurch是AD的潜在保护性因素。虽然APOE3ch突变的发现为AD的病理机制研究提供了全新视角,但是APOE3ch突变极为罕见使其无法在人源性样本中进行机制研究。
近期,清华大学药学院鲁白团队通过敲入APP基因致病性突变而建立了AD人源性类脑器官模型。该模型在时间维度依次呈现AD的关键病理特征,包括Aβ沉积、tau病理性变化、星形胶质细胞增生和神经元死亡,为研究AD发生发展机制和开发潜在的治疗靶点提供了重要工具。此外,研究人员使用该AD类脑器官模型揭示了载脂蛋白E基因APOE3ch突变对AD病理过程和神经退行性变化的保护作用(图1)。
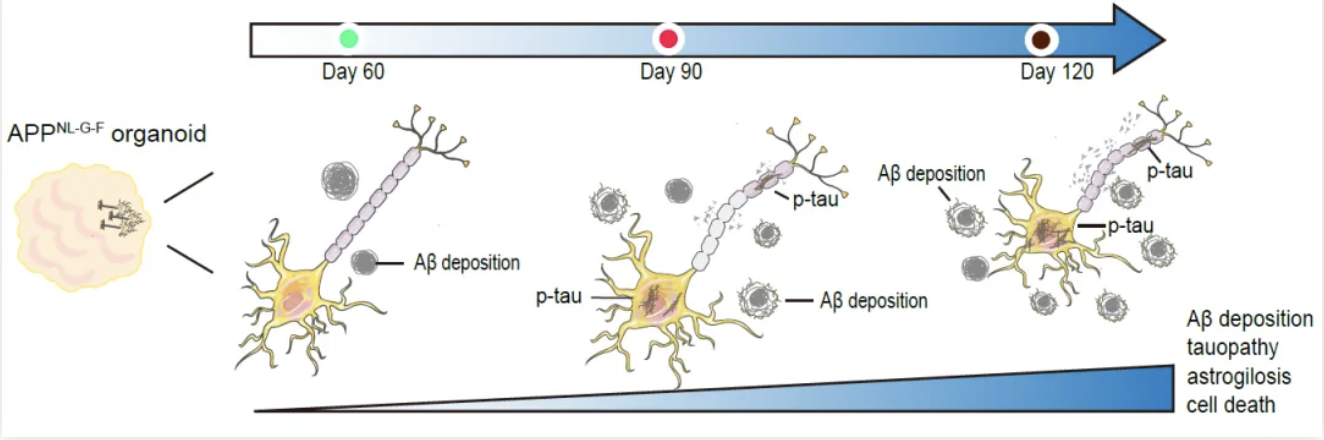
图1.APPNL-G-F人源性类脑器官模型在时间维度依次呈现AD关键病理特征
研究人员首先结合之前开发AD大鼠模型的经验,通过CRISPR-Cas9基因编辑将APP基因的3种家族遗传性致病突变引入人类H1胚胎干细胞(hESCs)中,证实了hESCs中发生了APPNL-G-F的纯合突变,并诱导分化为前脑类脑器官模型。研究人员在不同时间点检查了APPNL-G-F类脑器官模型的AD病理学特征,发现APPNL-G-F类脑器官Aβ42沉积显著增加,tau蛋白聚集增多,伴随星状胶质细胞增生。除了显著的AD病理学特征外,APPNL-G-F类器官中出现明显的细胞凋亡和坏死。
建立了人源性APPNL-G-F类脑器官模型后,研究人员利用该模型探究了APOE3ch对AD病理性变化和神经元死亡的潜在保护作用。通过CRISPR-Cas9基因编辑将APOE3ch敲入APPNL-G-FhESCs的基因组中,建立了表达APOE3(APPNL-G-F:APOE3)或APOE3ch(APPNL-G-F:APOE3ch)的AD类脑器官模型。研究人员利用上述类脑器官模型发现APOE3ch的表达显著降低了Aβ沉积,且减少了tau蛋白磷酸化和异常折叠。不仅如此, APOE3ch的表达有效缓解了APPNL-G-F类脑器官表现出的星状胶质增生和神经元死亡表型。可见,APOE3ch对于AD病理过程和神经退行性改变有显著的保护作用。
综上所述,本研究开发了一种新的人源性AD类脑器官模型(APPNL-G-F),该模型能在较短时间内高度模拟AD患者脑中出现的病理性改变及神经元死亡等特征。利用这一模型,研究人员证明了APOE3ch罕见突变对AD病理和神经退行性变的保护作用,为研究APOE3ch的生物学特点及其缓解AD的细胞和分子机制提供了新的工具。
值得一提的是,近期有两篇APOE3ch相关论文发表。在《细胞》(Cell)发表的研究中,研究者构建了人源APOE3chknock-in小鼠品系,将其与基于Aβ的APP/PS1小鼠杂交后发现,通过上调小胶质细胞的吞噬作用,APOE3ch缓解了X34+Aβ纤维聚集(非Aβ寡聚体),以及Aβ相关的tau病理特征。在《自然·神经科学》(Nature Neuroscience)发表的研究中,研究者将APOE3chknock-in到APOE4小鼠中,将其与tau转基因小鼠PS19杂交后发现,纯合APOE3ch解救了APOE4驱动的tau病理和星形胶质增生等表型。
除了与这两项研究同样证明了APOE3ch对AD病理性变化的保护作用之外,本研究还有几点重要贡献。首先,与上述两项研究不同的是,本研究使用的是完全人源化的类脑器官系统。第二,APPNL-G-F类脑器官模型是基于敲入而不是致病基因突变的过表达系统,因此避免了由于转基因表达引起的潜在非生理表型。此外,本研究开发的APPNL-G-F类脑器官模型出现了Aβ和tau病理特征、星形胶质增生以及神经元的凋亡和坏死,这些特征在APP/PS1小鼠或PS19转基因小鼠中难以全部重现,避免了小鼠模型的局限性,也突显了本研究开发新的人源性AD类脑器官模型的重要意义。
相关研究以“APOE3ch在人源性阿尔茨海默病类脑器官中缓解Aβ和tau病理特征和神经退行性改变”(APOE3ch alleviates Aβ and tau pathology and neurodegeneration in the humanAPPNL-G-Fcerebral organoid model of Alzheimer’s disease)为题,于4月12日发表于《细胞研究》(Cell Research)。
清华大学药学院2015级博士生刘航(已毕业)、北京大学医学部副研究员梅帆为该论文共同第一作者,清华大学药学院教授鲁白、梅帆为该论文共同通讯作者。研究得到国家自然科学基金、人脑保护高精尖中心、北京智源人工智能研究院、北京市自然科学基金的资助。
文章来源清华大学新闻,分享只为学术交流,如涉及侵权问题请联系我们,我们将及时修改或删除。
-
2025年智能光子学与应用技术国际学 06-10

-
2025年8月优质学术会议推荐 589

-
2025年第十二届能源与环境研究国际 400

-
2025年机械工程,新能源与电气技术 559

-
2025年计算机科学、图像分析与信号 553

-
2025年材料化学与燃料电池技术国际 493

-
第七届精神病学国际大会(CP 202 08-01

-
第七届老龄化与老年医学国际学术会议( 08-01

-
第十四届心理学与健康国际学术研讨会( 08-01

-
第七届测绘与地理信息国际研讨会(CS 08-01

-
第七届大气与海洋科学国际研讨会(SA 08-01

-
第十一届地质灾害研究与防治国际学术会 08-01

-
第十六届地质和地球物理学国际会议(I 08-01

-
第七届细胞科学与再生医学国际研讨会( 08-01

-
第七届合成生物学与生物医学国际研讨会 08-01

-
2025最新JCR分区及影响因子1939

-
好学术:科研网址导航|学术头条分468

-
《时代技术》投稿全攻略:一位审稿499

-
2025年国际期刊预警名单发布!600

-
2025年中科院期刊分区表重磅发3957

-
中科院已正式发布2024年预警期861

-
2025年度国家自然科学基金项目727

-
中国科协《重要学术会议目录(202733

-
2024年国家自然科学基金项目评1138

-
2024年JCR影响因子正式发布1214

-
吉林大学校长张希:学术会议中的提1391

-
SCI论文插图全攻略:从规范解析08-01

-
国际学术会议参加经验是怎么样的呢08-01

-
掠夺性会议是怎么进行判断的呢?—08-01

-
SCI论文投稿费怎么交?202408-01

-
IAASE 21096

-
河南理工大学 21052

-
邢台爱尔眼科医院 2010

-
临床泌尿外科杂志编辑部 17905

-
NBX 7849

-
重庆风雅会议服务有限公司 23081

-
IETP-Association 24060

-
北京千和展览有限公司 7847

-
武汉中会会议服务有限公司 23000

-
温州会议网 18036

-
江苏省南京市 2349

-
中国社会岩石力学工程 23058

-
IETP-Association 24050

-
国家传染病诊断试剂与疫苗工程技术 21245

-
上海交通大学安泰经济与管理学院 23144

-
东北大学秦皇岛分校 18178

-
福建省空间信息中心 21027

-
中国农学会 23159

-
深圳市汉威展览策划有限公司 17975

-
励鸿展览(上海)有限公司 8388



















 501
501













































