北京大学生命科学学院刘君团队开发FOCAS平台实现m6A修饰位点的全转录组功能解析
2026/01/08
在RNA修饰研究中,N6-甲基腺苷(m6A)被认为是真核生物mRNA上分布最广泛且功能多样的修饰形式之一[1]。大量研究表明,m6A可通过调控RNA的剪接、稳定性、翻译及降解过程,深度参与基因表达调控[2]。与此同时,m6A修饰也存在于多类非编码RNA中,比如染色质相关调控RNA(chromatin-associated regulatory RNAs,carRNAs),并参与染色质功能调控,进一步增加了全面理解m6A作用模式的复杂性[3]。现有研究策略主要依赖对m6A调节因子的全局性干预,这种方法难以区分不同RNA分子、不同修饰位点在不同细胞环境下的功能差异,从而限制了对m6A精细调控逻辑的深入解析。
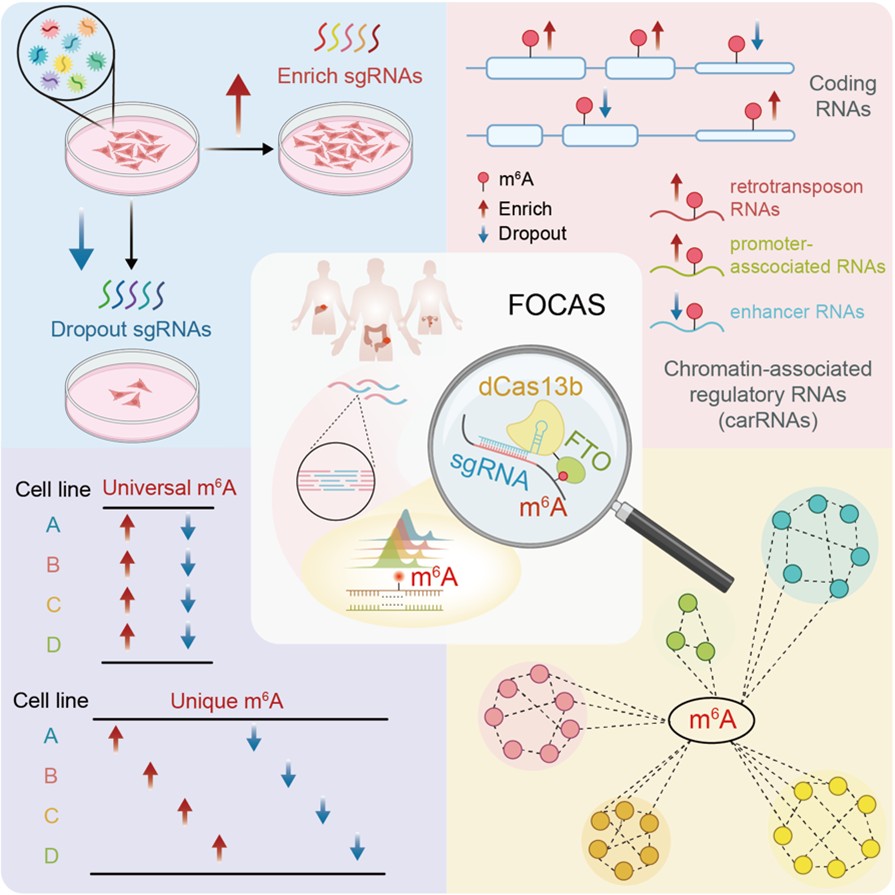
2025年12月31日,北京大学生命科学学院、北大-清华生命科学联合中心、北京大学核糖核酸北京研究中心刘君课题组在《细胞》(Cell)发表了题为“FOCAS:Transcriptome-wide screening of individual m6A sites functionally dissects epitranscriptomic control of gene expression in cancer”的研究论文。该研究建立了FOCAS(Functional m6A Sites Detection by CRISPR-dCas13b-FTO Screening)方法,实现了m6A功能研究在位点分辨率上的关键突破。FOCAS基于改造的CRISPR-dCas13b系统,将去甲基化酶FTO精准定位至RNA特定区域,从而在不改变DNA/RNA序列和不显著影响全局m6A水平的前提下,实现对特定m6A修饰位点的靶向去甲基化。这一策略不仅适用于mRNA,还可以同时覆盖非编码RNA,为在全转录组尺度上系统解析m6A的功能提供了技术基础。
论文截图
基于FOCAS策略,研究者在4种人类癌细胞系中系统评估了m6A修饰对细胞增殖能力的影响,共鉴定出4475个由m6A调控、显著影响细胞生长的功能基因。这些基因中的大多数此前未明确建立与m6A或肿瘤直接相关,提示m6A调控网络在癌细胞中的作用范围远超当前认知。进一步的位点层面分析揭示了m6A调控的高度异质性和基因背景依赖性。研究发现,即使在同一基因内部,不同m6A修饰位点也可能通过截然不同的机制影响RNA命运,从而对细胞表型产生相反的效应。这种差异主要源于不同m6A阅读蛋白的选择性结合。FOCAS使这种依赖于位点、阅读蛋白及细胞环境的m6A精细调控模式得以被系统揭示。
接下来,研究者使用FOCAS进一步探究了carRNA上m6A修饰的功能。结果显示,在3类carRNA——增强子RNA(enhancer RNAs,eRNAs)、启动子相关RNA(promoter-associated RNAs,paRNAs)及转座子来源RNA(retrotransposon RNAs,reRNA)上均鉴定出影响肿瘤增殖的关键m6A位点,表明carRNA上的m6A修饰同样具有重要的调控功能。进一步分析显示,在相同基因背景下,mRNA区域及其邻近的carRNA区域往往难以同时筛选到有效的sgRNA,而大部分携带关键m6A位点的carRNA,其邻近的编码基因与肿瘤特征具有更低的相关性。这些结果表明,携带m6A修饰的carRNA更倾向于通过反式调控作用发挥功能。
研究者系统比较了FOCAS在4种细胞系中鉴定的共性和差异性关键m6A峰(FOCAS-identified Peaks,FiPeaks),并据此将m6A调控模式划分为4种细胞系中都作用的“广泛型”(Universal-FiPeaks)与仅在特定细胞中作用的“特异型”(Unique-FiPeaks)两类。尽管多数m6A峰在4种肿瘤细胞系中均存在,但其往往仅在单一细胞系中调控肿瘤细胞生长,提示关键m6A位点的作用并非仅由修饰是否存在决定,而更取决于具体位点本身的生物学功能。对FiPeaks所在的RNA种类进一步分析显示,Universal-FiPeaks主要富集于mRNA,其所在基因在多种肿瘤中具有一致功能并与患者预后密切相关;而Unique-FiPeaks则更倾向富集于carRNA,表明非编码RNA上的m6A修饰在肿瘤类型特异性调控中发挥重要作用。这种功能分层为RNA修饰相关靶点的精准筛选和肿瘤特异性干预策略提供了重要理论依据。
值得注意的是,FOCAS进一步揭示了m6A修饰与转录调控网络之间的耦合关系。在肝癌细胞模型中,研究者鉴定出一组受m6A调控的关键转录调节因子,靶向这些基因上的修饰呈现“模块化”的调控特征,且同一模块内的转录表达谱表现出高度一致的变化模式。其中,KCTD1被鉴定为一个此前未被报道的、受m6A调控的潜在泛癌抑癌因子,并参与调控H3K4me3组蛋白修饰水平,显示出FOCAS在发现关键功能基因及作用机制方面的独特优势。
FOCAS方法鉴定肿瘤中全转录组关键m6A位点并解析其调控模式
综上所述,该研究通过FOCAS平台实现了对m6A修饰位点分辨率的精细调控功能的解析。研究结果表明,特定m6A位点本身即可作为精细的调控单元,深度参与基因表达调控及细胞命运决定。FOCAS不仅为理解m6A修饰的复杂调控逻辑提供了通用方法学框架,也为RNA修饰介导的肿瘤精准治疗研究奠定了重要基础。
刘君为本文的通讯作者。北京大学前沿交叉学科研究院2022级博士研究生张薪泞、北京大学生命科学学院2022级博士研究生张艺凡与2021级博士研究生刘欣宇为本文共同第一作者。北京大学生命科学学院魏文胜教授、胡婧研究员及同济大学高亚威教授为本工作提供了重要支持和贡献。本研究得到了国家重点研发计划、国家自然科学基金委、北京市自然科学基金委、北大-清华生命科学联合中心、北京大学生命科学学院及核糖核酸北京研究中心、基因功能研究与操控全国重点实验室和深圳湾实验室重点项目等项目和机构的支持。
文章来源北京大学,分享只为学术交流,如涉及侵权问题请联系我们,我们将及时修改或删除。
-
2026年6月优质国际学术会议推荐 7

-
2026年第17届机械与航空航天工程 193

-
2026年先进航空航天技术与卫星应用 324

-
2026资源、化学化工与应用材料国际 1808

-
2026年图像处理与数字创意设计国际 1632

-
2026年机械工程,新能源与电气技术 6095

-
2026年材料科学、低碳技术与动力工 1819

-
2026年艺术、文化产业与数字媒体国 04-29

-
2026年智慧教育、教育研究与文化交 04-29

-
2026年数字社会、公共管理与经济学 04-29

-
2026 政务服务、数字治理与智慧城 04-28

-
2026 制冷技术、暖通设备与环境调 04-28

-
2026 轻工材料、绿色制造与循环利 04-28

-
2026 多语言智能、翻译技术与国际 04-28

-
2026 生物育种、生态种植与现代农 04-28

-
中国科协发布2025年《重要学术12

-
2026年新锐分区(原中科院期刊2595

-
2025年两院院士增选有效候选人4402

-
2025最新JCR分区及影响因子12342

-
好学术:科研网址导航|学术头条分5673

-
2025年国际期刊预警名单发布!5837

-
2025年中科院期刊分区表重磅发20812

-
吉林大学校长张希:学术会议中的提6954

-
二维超导迈斯纳效应探测研究获进展04-29

-
研究发现笼目超导体中多重范霍夫奇04-29

-
二氧化碳加氢制高碳烯烃与航煤馏分04-29

-
靶向特定蛋白互作界面抑制乙肝病毒04-29

-
研究揭示内源信使调控膜损伤与细胞04-29

-
科学家绘制大脑星形胶质细胞转录因04-29

-
上海交大Bio-X研究院石毅与合04-29

-
北京北发电子商务股份有限公司 18333

-
老大哥寺院地 18455

-
太原理工大学 2804

-
凤人会议有限公司 21310

-
广东省生物医学工程学会 2413

-
中国国际经济发展促进会 19057

-
湖南科技大学 21300

-
武汉英奇会展有限公司 8374

-
第二届2017机械控制与自动化国 24360

-
丽江大港旺宝国际饭店 23233

-
上海信世展览服务有限公司 8954

-
济南大学 21449

-
山东泉得利环保科技有限公司 24453

-
环球科研协会(GSRA) 24467

-
吉林省北华大学师范分院美术系 21281

-
长春广信会务服务有限公司长春招商 18299

-
中国市政工程协会 18403

-
北京久久国际会展有限公司 24507

-
未来之星 21449

-
国际工学技术出版协会 24370






















 117
117